乳铁蛋白及乳铁蛋白生产杀菌的稳定性介绍
王瑞宝
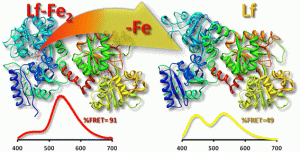
乳铁蛋白(Lactoferrin, LF)是转铁蛋白家族中的一种铁结合糖蛋白,存在于人体的乳汁和各种分泌液中,以母乳中的含量最高。人LF 和牛LF 氨基酸序列具有69%的同源性,因此二者具有相似的生物活性。LF 具有抗微生物、促进肠道发育、促进铁吸收、免疫调节等功能。LF 是母乳中重要的活性蛋白。现有的人群研究结果显示,LF可预防和辅助治疗婴幼儿腹泻、新生儿坏死性小肠结肠炎、呼吸道疾病、新生儿败血症,对改善婴幼儿贫血和促进其生长发育也有一定的作用[1]。
LF在加热时会发生不同程度的变性,变性程度主要与加热时间、pH值和铁饱和度等有关,巴氏消毒以及冷冻储存等手段都会在一定程度上降低LF的含量和活性。同样,在乳制品加工过程中,如脱脂乳、乳清以及乳蛋白的分离过程中,由于受到高压处理,其中的LF也会大量发生变性[2]。
乳铁蛋白(LF)对热敏感.容易变性失活。关于乳铁蛋白的热稳定性,已有一些研究报道。HIROAKI等[3] 研究了在酸性条件下牛乳铁蛋白的热稳定性.发现脱铁乳铁蛋白在酸性条件下非常稳定 CELIA等[3]研究了热对LF抑菌活性的影响.发现85℃ 保温10 min的热处理强度未降低LF的抑菌活性 LUIS等[4]研究发现72℃ 保温20 s~ 135℃ 保温8 s的热处理条件几乎不影响LF的铁结合能力.然而两种温度下更长的时间则会降低铁结合能力。MARIE-~I4]研究了不同铁饱和度的LF;f~巴杀和uHT后的结构和抑菌活性变化. 发现uHT造成LF的完全变性。
采用非还原电泳定量可以很好的反映乳铁蛋白受热损失的情况。63 ℃ 30 min的热处理后,LF形成了少量的聚集体. 72 ℃( 15 s) 的热处理条带与未热处理的LF几乎相同,这种热处理条件对LF造成的损害是最小的。85 ℃( 15 s)热处理后LF也形成了少量不能进入分离胶的聚集体但聚集体的数量少于63 "C(30 min) 的。而85℃(10 min) 和95 ℃ (5 min) 热处理
后, LF除形成了不能进入分离脏的聚集体外,还形成了更大的不能迸入浓缩脏的聚集体, 95 ℃(5 min) 对LF造成的损失明显高于85 ℃( 10 min)和 UHT后LF几乎全部形成了很大的聚集体,这种聚集体影响了LF的生物活性和铁结合稳定性。
乳铁蛋白对杀菌热敏感,温度上升和杀菌时间延长都能显著的破坏乳铁蛋白活性,对温度的上升比时间的增加更加敏感。优选的杀菌温度为85℃ 5min,尽量不要使用UHT杀菌,会大幅度破坏乳铁蛋白结构。
乳铁蛋白是热敏性物质.乳制品加工中的各种常规热处理都会或多或少造成乳铁蛋白结构或生物活性的改变,乳铁蛋白所遭受的热处理强度越高。则变性和失活的程度也越高 特别是乳铁蛋白在遭受UHT等强热处理后,其特征电泳条带损失很大.自由巯基和表面疏水性变化也指示乳铁蛋白结构发生了显著改变.同时铁结合能力和抑菌活性这两大乳铁蛋白主要的生物活性也降低很多。但巴氏杀菌对乳铁蛋白结构及生物活性的影响较小 因此在乳铁蛋白生产和应用过程中。应该尽量减少乳铁蛋白受到强度较高的热处理。以保证乳铁蛋白的优良生物活性得到较好保留.
参考文献:
[1]. 中国营养学会妇幼营养分会. LF 乳铁蛋白婴幼儿健康效应专家共识. 临床儿科杂志, 2018, 36(11):884-887.
[2]. 闰序东,王彩云,云战友. 乳铁蛋白热稳定性研究. 中国乳品工业, 2014, 42(4):19-20.
[3].HIKOAKI A,HITOSHI S,HIKOSHI M,et al.Heat stability of Bovine Lactoferrin at Acidic pH[J].J.Dairy Sci.,1991,74(1):65—71.
文章评论(0)